Na2S2O3 + 2HCl = 2NaCl + S + SO2 + H2O

Соляная кислота – это водный раствор газообразного хлороводорода HCl. Массовая доля хлороводорода в соляной кислоте не может превышать 37 % из-за ограниченной растворимости газов в воде. Соляная кислота называется так потому, что получили ее впервые из поваренной соли прокаливанием ее с железным купоросом FeSO4 ∙ 7H2O:
2(FeSO4 ∙ 7H2O) + 2NaCl = 2HCl + Fe2O3 + Na2SO4 + SO2 + 13Н2О
Этим способом монах-алхимик Василий Валентин в XV в. получил пары, которые при растворении в воде дали то, что мы сейчас называем соляной кислотой, а Василий Валентин назвал spiritus salis (дух соли). Арабским алхимикам этот способ был известен несколькими веками ранее.
Немецкий химик Иоганн Рудольф Глаубер в середине XVII в. заменил в этом рецепте железный купорос на концентрированную серную кислоту и получил значительно более чистую соляную кислоту:
2NaCl + H2SO4 = 2HCl + Na2SO4

В реторте после отгонки соляной кислоты оставалась соль, которую Глаубер растворил в воде и исследовал. Оказалось, раствор соли обладает слабительным действием. Глаубер назвал ее Sal mirabile (удивительная соль). До сих пор ее используют в медицине под названием «глауберова соль». А природный кристаллогидрат Na2SO4 ∙ 10Н2О назвали мирабилитом. По способу Глаубера соляную кислоту получали еще в ХХ в. Надо полагать, именно такую кислоту купил в аптеке Валя Катаев.
И цинк с примесями, и оцинкованное кровельное железо прекрасно взаимодействуют с кислотой с образованием водорода. Кстати, цинк с примесями свинца и других менее активных металлов с кислотой взаимодействует значительно быстрее, чем химически чистый цинк. Контакт двух металлов разной химической активности в растворе электролита создает так называемую гальваническую пару, в которой более активный металл (в данном случае цинк) окисляется быстрее, а менее активный, наоборот, не окисляется, пока сосед «отвлекает на себя» ионы водорода, выступающие в роли окислителя. Поэтому гранулы цинка, побывавшие в пробирке с кислотой, как бы чернеют: светлый блестящий цинк растворяется, а на поверхности выступают темные кристаллики свинца, висмута и других примесей, не растворяющихся в соляной кислоте. Но почему тогда загрязненный цинк не рекомендуют брать для получения водорода? А потому что примесями к цинку могут быть не только менее активные металлы, но и мышьяк, фосфор, сера. Атомарный водород в момент выделения восстанавливает эти примеси до летучих водородных соединений арсина (AsH3), фосфина (РН3), сероводорода (Н2S). Все эти соединения представляют собой ядовитые газы с неприятными запахами. У чистого арсина нет запаха, но загрязненный имеет чесночный запах. Фосфин обладает «запахом гнилой рыбы», а сероводород имеет «запах тухлых яиц». Он-то, видимо, и выделялся вместе с водородом в опыте гимназиста Катаева, «слегка пованивая чем-то тухлым». Значит, цинк, проданный в аптеке, тоже был загрязнен примесями серы или сульфидов, и опыт был не вполне безопасен. Чтобы очистить водород от примеси ядовитых газов, нужно было бы пропускать его через раствор какого-нибудь окислителя, способного окислить эти газы до безвредных солей. Например, через подкисленный раствор дихромата калия или перманганата калия. А поместить этот раствор следовало бы в двугорлую промывную склянку (склянку Вульфа), соединенную газоотводной трубкой с той склянкой, где бесстрашный экспериментатор получал водород.
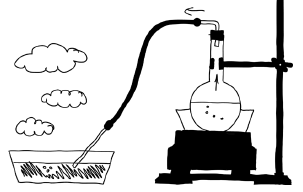
Восторг, который охватил гимназиста Валентина в магазине лабораторного оборудования, понятен. Стеклянная химическая посуда завораживает совершенством своих форм. Многое из того, чем в начале ХХ в. любовался и даже пользовался незадачливый экспериментатор, изобретено за сотни лет до описываемых событий и до сих пор встречается в химических лабораториях. «Специальный сосуд для соединения цинка с кислотой» – это аппарат Киппа, которым и сейчас пользуются в школьных химических лабораториях. Раньше его форма ассоциировалась у учеников со снеговиком, а сейчас они чаще при взгляде на аппарат Киппа вспоминают кальян. Прибор этот с середины XIX в. производила голландская фирма научных приборов, принадлежавшая аптекарю Петеру-Якобу Киппу, отсюда его название. В аппарате Киппа получают газы действием какого-либо раствора на твердое вещество, если для реакции не требуется нагревание. Прибор устроен таким образом, что при перекрывании газоотводной трубки избыток газа выдавливает кислоту в сферическую воронку и реакция прекращается. Стоит открыть кран, и газ выходит из сферического резервуара, давление в нем падает, кислота возвращается туда, где находится цинк, и снова начинается выделение водорода. То есть реакцию можно в любой момент как остановить, так и возобновить. Это очень удобно и экономно. Но у Валентина не было денег на такой дорогостоящий прибор.
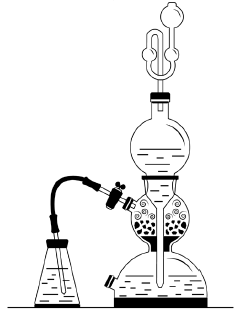
Двугорлая реторта, восхищавшая юного естествоиспытателя, не предназначена для получения водорода. Как и колба, и в отличие от аппарата Киппа, реторта изготовлена из тонкого жаропрочного стекла и предназначена для нагревания веществ. Но отогнутый вниз носик реторты позволяет сконденсировать образующиеся пары и собрать конденсат в колбочку. Реторту использовали для перегонки или отгонки летучих веществ. Алхимики пользовались ретортами с незапамятных времен, и до сих пор их выпускают стеклодувные мастерские.
Горелка Бунзена, названная так в честь немецкого химика Роберта Бунзена, была описана им в одной из публикаций в середине XIX в. Она предназначена для сжигания газообразного топлива, чаще всего природного газа. В Одессе до 1962 г. не было газопровода от месторождения природного газа. Правда, в 1865 г. в городе был построен газовый завод, на котором из каменного угля, поставлявшегося морем из Кардиффа, производился искусственный светильный газ (смесь водорода, угарного газа и метана). Но искусственный газ использовался в основном для освещения улиц газовыми фонарями. На кухнях горожане готовили в печках или на керосинках. Следовательно, подводки газа в семье Катаевых не было, и покупка горелки практического смысла не имела. Для получения водорода горелка и не нужна, но может пригодиться при испытании водорода на чистоту.
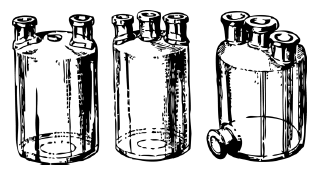
Двугорлая банка, на которой в конце концов и остановился гимназист Валя, называется промывной склянкой Вульфа. Она сконструирована в XVIII в. английским химиком Питером Вульфом и предназначена для промывания или осушения газов. В склянку наливают на четверть объема промывную или осушающую жидкость. Газ поступает в склянку через одно из отверстий. В горлышко вставлена пробка с газоотводной трубкой, опущенной в жидкость. Пробулькивая через жидкость, газ очищается от примесей, а затем выходит из другого отверстия. Но можно использовать склянку Вульфа и для других целей, например для получения водорода.
Приступая к опыту, Валентин Катаев знал о взрывоопасности смеси водорода с кислородом или с воздухом. Аптекарь предупредил его о неизбежности образования гремучего газа. Гремучим газом называют смесь водорода с кислородом, взрывающуюся при поднесении к ней пламени. Гремучей является любая смесь горючего газа с кислородом или воздухом. Например, причиной аварий в угольных шахтах обычно является взрыв гремучей смеси рудничного газа (метана) с воздухом.
Не любая смесь водорода с кислородом или воздухом способна взрываться. Если в гремучем газе соотношение объемов водорода и кислорода равно 2:1, взрыв будет наиболее мощный. При изменении пропорций сила взрыва уменьшается, а если водорода в смеси менее 3 % или более 92 %, она не воспламенится. Для смеси водорода с воздухом наиболее сильный взрыв произойдет при 28 % водорода, а если водорода менее 4 %, она не загорится. В отличие от метана, водород практически не встречается в природе, но со взрывом гремучего газа тоже могут быть связаны несчастные случаи, от взрывов в лабораториях до происшествий на производстве.
История исследования водорода начинается после 1766 г., когда он был открыт английским химиком Генри Кавендишем. Обнаружилось, что газ этот чрезвычайно легкий и горючий. Рассказывают, что французский химик, пионер воздухоплавания Жан Франсуа Пилатр де Розье решил проверить, что будет, если вдохнуть водород. Наполнив легкие водородом, он выдохнул его на пламя свечи. Как и гимназист Катаев, он думал, что водород просто сгорит на воздухе. К сожалению, в легких водород смешался с воздухом, гремучий газ при соприкосновении с пламенем воспламенился, огонь распространился (как и в опыте Вали Катаева) на весь объем смеси, находящейся в легких, и произошел взрыв! Пилатру де Розье показалось, что все его зубы вылетели вместе с корнями. Но в этот раз бесшабашный химик остался в живых. И все же именно несчастный случай с участием водорода стоил ему жизни.
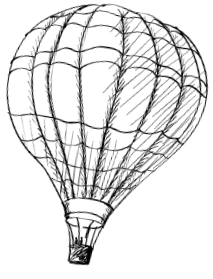
Здесь нужно немного вспомнить историю воздухоплавания. Братья Монгольфье в 80-е гг. XIX в. изобрели воздушный шар, поднимающийся в атмосфере благодаря наполнению теплым воздухом. Сначала была идея наполнить шар водородом, но не удалось создать герметичную оболочку для газа, молекулы которого легко проходили сквозь ткань. Одновременно с братьями Монгольфье над проблемой воздухоплавания работал французский физик Жак Шарль. Он, как и братья Монгольфье, решил наполнять шар легким газом водородом, но сумел решить проблему проницаемости оболочки: пропитал ткань раствором каучука в скипидаре, сделав ее газонепроницаемой. Испытание шарльера произошло несколькими месяцами позже монгольфьера. Пилатр де Розье увлекся воздухоплаванием и решил объединить достоинства монгольфьера и шарльера в одном аэростате с двумя оболочками, в одной из которых содержится водород, а вторая в ходе полета наполняется горячим воздухом. Такой аэростат должен был обладать большей маневренностью. Но соседство горючего водорода и открытого пламени привело к трагедии. Во время пробного полета розьера через Ла-Манш искра из нижней оболочки попала в верхний баллон с водородом, аэростат загорелся, Пилатр де Розье и его спутник погибли вместе с аэростатом.
Эта катастрофа была не последней в истории воздухоплавания, связанной с водородом. Уже в XIX в. были созданы дирижабли – летательные аппараты легче воздуха, оснащенные двигателем. Их наполняли самым легким газом, водородом. В Германии в первой половине ХХ в. широко использовались дирижабли конструкции графа Фердинанда фон Цеппелина, называвшиеся в честь него цеппелинами. Эти дирижабли, наполняемые водородом, были задействованы в пассажирских перевозках, в частности, совершали трансатлантические рейсы. В 1937 г. завершивший перелет из Германии в США цеппелин «Гинденбург» погиб у причальной мачты на базе Лейкхерст от возгорания и взрыва баллонов с водородом. После этой трагедии дирижаблестроение сошло на нет, а дирижабли были вытеснены самолетами.
Хотя аптекарь и предупредил юного экспериментатора о гремучем газе, но его совет о том, как избежать взрыва, никуда не годится. Визуально определить, когда весь воздух будет вытеснен и из трубочки пойдет чистый водород, невозможно. Единственный надежный способ – испытывать водород на чистоту перед применением. Этот способ описан в каждом учебнике химии. Надо собрать порцию выделяющегося водорода в перевернутую вверх дном пробирку и поднести ее, не переворачивая, отверстием к пламени. Если раздастся легкий хлопок, значит, водород чистый и можно его поджигать. Если в пробирке гремучий газ, раздастся резкий свистящий звук. Надо подождать, а потом провести испытание еще раз, и так до появления легкого хлопка.

Тем, кто сталкивается в лаборатории с водородом, очень полезно прочитать детальное описание его взрыва, которое сделал наблюдательный, но беспечный гимназист Валя Катаев. После этого рассказа уже не забудешь об испытании водорода на чистоту!