Чому зебри не страждають на виразку
Такі захисні механізми імунної системи зумовлені цілим набором клітин крові, що називаються
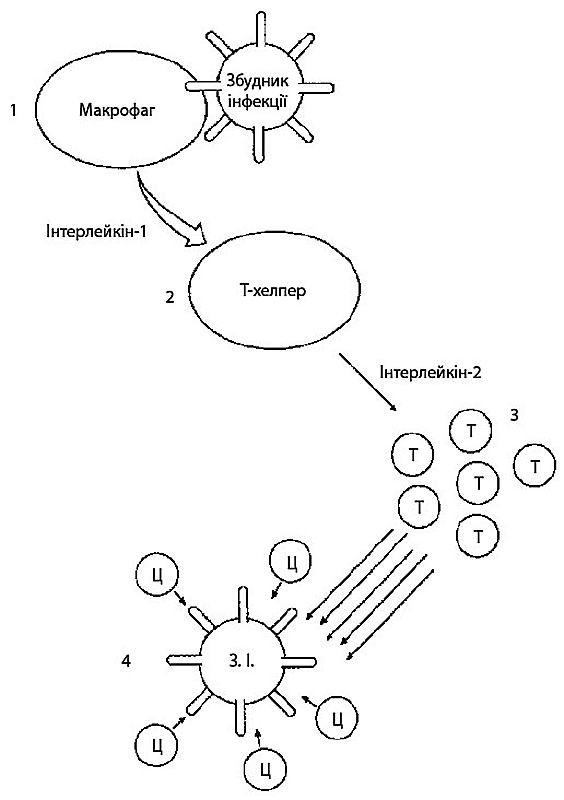
Т-лімфоцити і В-лімфоцити по-різному атакують збудників інфекційних захворювань. Т-лімфоцити допомагають утворити клітинний імунітет (див. ілюстрацію на с. 144). Коли джерело інфекції потрапляє в організм, його виявляє різновид моноцитів під назвою макрофаг, який сповіщає про появу чужака клітину Т-хелпера. Лунає уявна сигналізація, і Т-лімфоцити починають множитись у відповідь на вторгнення. Ця сигналізація, зрештою, активує також і розмноження цитотоксичних Т-лімфоцитів, які нападають і ліквідують збудника інфекційної хвороби. Вірус СНІДу знищує саме Т-лімфоцити.
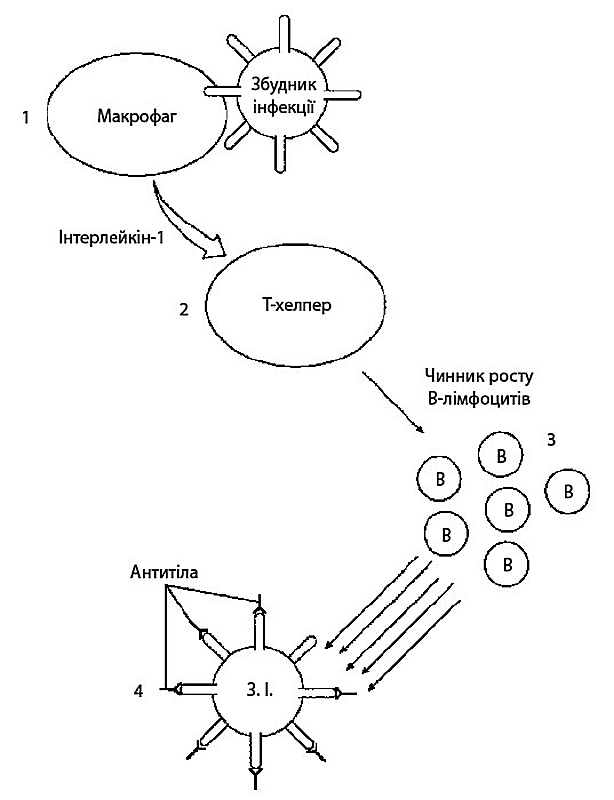
На противагу, В-лімфоцити формують гуморальний імунітет (див. ілюстрацію на с. 145). Коли відбувається співпраця між макрофагом і Т-хелпером, клітини Т-хелпера стимулюють розмноження В-лімфоцитів. Основним завданням В-лімфоцитів є розрізняти клітини та генерувати антитіла — великі білкові сполуки, які розпізнають та приєднуються до якоїсь специфічної частини збудника інфекційної хвороби, який проник в організм (як правило, до поверхневого білка мембрани). Ця особливість надзвичайно важлива — вироблені антитіла мають унікальну форму, яка допомагає ідеально прикріпитися до збудника — наче ключ вставляється в замок. Так антитіла іммобілізують збудників інфекційного захворювання і знищують їх.
Імунна система має ще одну особливість. Наприклад, якщо різні частини печінки мають скоординувати якийсь процес, вони користуються своїм зручним сусідством одна з одною. Але імунна система простягається по всій системі кровообігу. Для того щоб увімкнути імунну «сигналізацію» по всій цій розгалуженій системі, в організмі функціонують хімічні месенджери, які переносяться з кров’ю і встановлюють зв’язок між різними видами клітин —
Як правило, імунна система досить вправно відрізняє своїх від чужих (хоча підступні тропічні паразити, як-от ті, що викликають шистосомоз, призвичаїлися обманювати людську імунну систему, маскуючись під клітини організму). Наша імунна система просто насолоджується процесом сортування: червоні кров’яні тільця — це наші хлопці, брови — теж наші, вірус — стоп! Атакувати; м’язові клітини — все гаразд, наші.
Але раптом під час процесу сортування станеться збій? Найочевиднішою помилкою імунної системи є дозвіл збуднику інфекції зайти до організму — звичайно, це прикрість. Але однаково прикро буде, якщо імунна система сприйме за небезпечного загарбника щось, що ним не є. Як один із варіантів такого сценарію, сигнал тривоги у вашому організмі може викликати якась геть безневинна річ, яка туди потрапила. Може, це звичний для вас продукт, наприклад, арахіс чи креветки, або якась сполука, що передається повітряним шляхом, як квітковий пилок. Проте ваша імунна система вирішить, що до організму потрапило не тільки щось стороннє, але й небезпечне, і запустить механізм реакції. Так виникає алергія.
У другому варіанті гіперреакції імунна система сприймає якусь частину організму за збудника інфекції і атакує її. Якщо імунна система помилково атакує нормальну частину організму, може виникнути ряд жахливих «аутоімунних» захворювань. Наприклад, за розсіяного склерозу під приціл попадає частина нервової системи, а за ювенільного діабету — клітини підшлункової залози, які виробляють інсулін. Як ми незабаром дізнаємося, стрес справляє досить неоднозначний вплив на перебіг аутоімунних захворювань.
Поки що зосередимося на понятті
Набутий імунітет — це досить хитромудрий винахід і притаманний лише хребетним. Але ми також маємо і простішу, більш давню форму імунної системи, яку поділяємо з такими далекими від нас видами, як-от комахи, а саме —
Така імунна реакція загального характеру, як правило, виникає на підступах до організму — наприклад, коли патоген уражає шкіру або слизову оболонку рота чи носа. Як перший запобіжник, у слині міститься клас антитіл, які атакують будь-який клас мікробів на своєму шляху, не виробляючи зброю індивідуально проти кожного чужака. Ці антитіла виробляються та вкривають слизові оболонки нашого організму як антисептичний засіб. До того ж, на ділянці, ураженій інфекцією, розходяться капіляри, дозволяючи клітинам вродженої імунної реакції швидко вийти з кровообігу і проникнути безпосередньо в місце ураження. Серед таких клітин —
Ми вже маємо загальне уявлення про діяльність імунної системи організму. Тепер час розібратись із впливом стресу на імунітет. Як виявляється, він набагато більш комплексний, ніж здається.
ЯК СТРЕС ПРИГНІЧУЄ ІМУНІТЕТ
Майже 60 років тому Сельє отримав перші докази пригнічення імунітету внаслідок стресу, встановивши, що частини імунної системи на кшталт тимусу атрофувались у щурів, які опинились у неспецифічній неприємній для них ситуації. Відтоді науковці дізналися про більше особливостей діяльності імунної системи — виявилося, що стрес може суттєво послабити імунітет.
Стрес призупиняє утворення нових лімфоцитів та їх викид у систему кровообігу та скорочує тривалість перебування вже вироблених лімфоцитів у крові. Це порушує вироблення нових антитіл у відповідь на появу збудника інфекції та пошкоджує комунікацію між лімфоцитами через відповідних месенджерів. І все це позначається на реакції вродженого імунітету, не даючи розвиватися запальному процесу. Таке відбувається внаслідок впливу будь-якого виду стресогенних чинників (фізичних та психологічних) в організмі приматів, щурів, птахів і навіть риб. Звичайно, і в людському організмі також.
Найкраще такий процес пригнічення імунітету видно на прикладі глюкокортикоїдів. Зокрема, глюкокортикоїди можуть зумовити зменшення розміру тимусу; це настільки перевірений взаємозв’язок, що в давні часи (близько 1960 року) до того, як стало можливим точно виміряти кількість глюкокортикоїдів у крові, одним з непрямих способів зробити це було просто перевірити, наскільки сильно зменшився тимус у тварини. Що менший тимус, то більше глюкокортикоїдів у крові. Глюкокортикоїди зупиняють утворення нових лімфоцитів у тимусі, а тканина тимусу здебільшого складається з цих нових клітин, готових влитися у систему кровообігу. Оскільки глюкокортикоїди припиняють вироблення таких месенджерів, як-от інтерлейкіни та інтерферони, вони також зменшують чутливість лімфоцитів у крові до інфекції. Більше того, глюкокортикоїди виводять лімфоцити з системи кровообігу і змушують їх накопичуватись у тканинах органів імунної системи. Переважно глюкокортикоїди діють проти Т-лімфоцитів, а не В-лімфоцитів. Це означає, що клітинний імунітет слабне більше за гуморальний. І що вражає найбільше, глюкокортикоїди можуть фактично знищувати лімфоцити. Це підводить нас до найактуальнішої теми сучасної медицини — запрограмованої загибелі клітин[59]. Інколи клітини програмують себе на самознищення. Наприклад, якщо клітина починає перетворюватися на ракову, режим самознищення активується для того, щоб запобігти неконтрольованому поділу; декілька видів раку характеризуються тим, що немає механізму запрограмованої загибелі клітин в організмі хворого. Виявляється, що саме глюкокортикоїди можуть призвести лімфоцити до самознищення в різні способи.
Гормони симпатичної нервової системи, бета-ендорфіни та КРГ у мозку також відіграють свою роль у пригніченні імунітету під час стресу. Механізми цього впливу далеко не так добре досліджені, як пригнічення імунітету глюкокортикоїдами, і взагалі вплив цих гормонів на імунну систему традиційно вважали слабшим за вплив глюкокортикоїдів. Однак низка експериментів показали, що стресогенні чинники все ж таки можуть пригнічувати імунітет незалежно від секреції глюкокортикоїдів.